
話し手:名古屋文理大学・健康生活学部
教授 清水 俊雄 氏
聞き手: 医療経済研究機構
専務理事 岡部 陽二
今回は、名古屋文理大学健康生活学部教授の清水俊雄氏に健康食品の普及啓発と信頼性向上に向けての取組みについてお伺いしました。
健康食品は年間売上げ2兆円の市場規模に達していますが、そもそも「健康食品」とは何か、「食品一般」や「医薬品」とどう違うのか、有効性や安全性は制度的にどのようにして担保されているのか、これらの点は一般の消費者にはよく分かりません。食の機能と安全の分野では、ことのほか科学に基づいた制度と制度を支える科学が必要ですが、いずれもわが国だけではなく世界的に見ても発展途上の段階にあります。そこで、消費者が安心して健康食品を購入できるように、その環境整備に腐心してこられた清水俊雄先生から、そのあたりの事情とご苦労をじっくりとお聞きしました。
清水俊雄先生は、東京大学農学部農芸化学科卒業、生物化学専攻で農学博士、旭化成㈱において機能性食品やバイオテクノロジー食品の研究開発に20年あまり携わられ、その間、厚労省へ機能性食品の制度化へ向けての提言など産学官に亙っての活発な活動を行なってこられました。
2008年には食品の健康と安全に関するコンサルティング業務を自ら手掛ける「フレスコ・ジャパン」を設立して代表取締役に就任、2006年から現職の傍ら日本臨床栄養協会サプリメント・アドバイザー認定機構理事・教育資格委員長、(独)国立健康・栄養研究所栄養情報担当者(NR)認定委員会委員、日本臨床栄養協会理事など多数の役職に就いておられます。
著書には「特定保健用食品の開発戦略」(日経BP社)、「機能性食品素材便覧」(薬事日報社)、「食品機能の制度と科学」、「特定保健用食品の科学的根拠」(ともに同文書院)ほか多数があります。
〇レギュラトリー・サイエンス(Regulatory Science)の意義
岡部 食品と医薬の関係というか、それぞれの領域はどうなっているのか、医食同源と言われますが、医薬と食品がどういう基準で区分されているのか、素人にはよく分かりません。医薬の分野では、薬害問題などもあって、法制面でも整備が進んでいますが、食品の機能と安全の分野でも「科学に基づいた制度と制度を支える科学、すなわちレギュラトリー・サイエンス(Regulatory Science)が重要である」という先生の問題意識には説得力があります。
清水 私は大学での専門は、「食品のレギュラトリー・サイエンス」としておりますが、もともとは旭化成でバイオテクノロジーの中で、細胞融合とか、遺伝子組換えを実施して、植物から有用物質を生産しようと考えたのが研究のスタートでした。微生物からですと医薬品の方にどんどん行くのですが、植物からですと、なかなか成長が遅いということもあって、対象を食品に定めました。
岡部 機能性を持った成分の食品を植物から作る研究ですね。もともと、食品というのは植物または動物からつくられるものですから、ことさらに、有用物質とか機能性という概念を創り出して、一般に理解させるのは難しいですね。
清水 私が食品の機能の研究を始めたのは、1980年代初めでした。ちょうどその頃に、東大の藤巻先生と京大の千葉先生という方が中心になって、文部科学省の科研費で、機能性食品の特定研究が始められました。ただ、この研究の成果を実際に社会に役立てようと考えて、この食品は健康によい、こういう機能を持ったものであるということを表示しようとすると、薬事法に触れて法律違反だと言われる障害にぶつかりました。
岡部 薬事法の中に「体の構造と機能に影響を及ぼすことを目的としているものは、医薬品として規制する」ということが書いてあるわけですね。ただ、医薬には病気を治す機能はありますが、健康を増進する機能は、食品にしかないのではないでしょうか。
清水 そうです。よく考えてみると、ただ今お話しすることを考えたりする脳の機能というのは朝、食べた炭水化物、グルコースが唯一のエネルギー源となっています。手の筋肉、骨も決して薬を摂取してできているわけではなくて、毎日、食べている食品の機能によっているわけです。逆に言うと体の構造と機能に影響を及ぼさない食品は存在しないと言ってもよいのですが、薬事法では体の構造と機能に影響を及ぼすものは医薬品だとしているのです。
一方で、食品とは何かという定義が食品衛生法の中にあり、この法律で食品とはすべての飲食物を言うと書いてあるのです。
岡部 機能性食品の部分は、二つの法律でダブっているわけですね。
清水 そうです。ただし、食品衛生法には、「薬事法で定める医薬品と医薬部外品を除く」という但し書きが付いています。その結果、わが国では、体の構造と機能に影響を及ぼすものはすべて医薬品として薬事法で取り締まれるという法体系となっているのです。ですから、ある食品によい機能を発見したり、それをエンリッチした食品をつくったりしても消費者に伝えられないのが問題でした。
また、健康機能というのは食べてすぐに分かるものではありませんから、結局、機能を表示しなければ、世に出せないのです。食品の機能をエンリッチするのには、お金もそれだけ掛かるわけですから、一定の表示をして、消費者に伝える手段がないと、コストが高くなった分を補えません。1984年に国家プロジェクトが始まって、企業も一生懸命に開発を始めたのですが、ビジネスとして成り立たないわけです。
そういう問題が一挙に出てきたので、1980年代の後半くらいから機能性食品を法律の中できちんと位置づけようという動きが出てきて、91年に食品の中でも「特定保健用食品(トクホ)」だけが、薬事法で定められている体の構造と機能に影響を及ぼすものの例外として、その機能表示ができるように法律で制度化されたのです。これが、いわゆる「トクホ」と言われているものです。
岡部 なるほど、トクホの誕生には大変なご苦労をされてきたのですね。
清水 食品の機能について、いくら科学的に研究をして、それを深めて、有用なものを開発したとしてもレギュレーションができていないと、それを世の中に活かせないということです。
岡部 レギュレーションがないと、折角のサイエンスが生かせず、研究の意味がないわけですね。
清水 レギュレーションができたおかげで、今まであまり興味を示さなかった企業もトクホの研究をやろうということで、サイエンスが更に盛り上がるのです。このレギュレーションとサイエンスというのはまさに車の両輪として、両方が重要です。片方だけが前に進んでも、それは全体としてはうまくいかないということです。私はレギュラトリー・サイエンスの重要性を主張してきましたが、国際学会の中でも、法律の議論と機能性食品というサイエンスの議論はばらばらでした。今後の課題としては、法律としての国際的整合性が必要と痛感しています。
岡部 レギュラトリー・サイエンスというのは何も食品の機能を評価するためだけに有用ではないわけですね。日本がリードしているiPS細胞(人工多能性幹細胞)の分野でも、レギュレーションがないために研究が遅れるといった問題が出てきているようですが。
清水 そうです。もちろん、いろいろな分野でレギュレーションとサイエンスの併進が重要ですが、とくに食品はサイエンスだけが前に進んで、レギュレーションがまったく存在しない状況が続いていたわけです。食品の場合には、30年くらい前にそれが露呈してきたのです。
「機能性食品」という日本語を"functional food"というふうに英訳しましたが、1990年代の前半でも、欧州では、圧力をかけて肉を押し出してソーセージにするような物理的機能を変えた食品のことをファンクショナル・フードと言っていました。それを彼らは "physical functional food"という意味で昔から使っていたのです。
われわれは食品の「ファンクション(機能性)」と言えば健康によいという機能を指すものと考えていたのですが、欧州ではもともとこういう意味で使っているのだとの話もあり、仕方なく「機能性食品」は"physiological functional food"(PFF)と訳すことにしました。
ところが、2000年以降、「ファンクショナル・フード」といえば、米国でも欧州でも、すべて日本の定義通りに統一されました。ですから、ファンクショナル・フードというのは、日本発の学術用語です。これは、一般にはあまり知られていない事実です。
岡部 それはまた大変なことですね。カラオケとかスシとかと同様ですね。
〇健康食品の定義
岡部 健康食品の市場規模は年間売上げ2兆円に達していますが、そもそも「健康食品」とは何か、「食品一般」や「医薬品」とどう違うのか、その範囲の定義、健康食品の分類方式などについてご説明ください。
清水 健康食品についての法律的な定義はありません。一般的には、図1に示しましたように、食品というカテゴリーの中に、「特定保健用食品(トクホ)」と「栄養機能食品」が法律的に定められたカテゴリーとしてあります。トクホは個別の商品ごとに評価して表示が許可されたもので、栄養機能食品は規格基準があって、それに従えば栄養機能表示ができるカテゴリーのものです。このいずれにも当てはまらないもので健康に良いと標榜される食品が、健康食品と称して販売されている「いわゆる健康食品」も存在します。
岡部 一方、先生の「機能性食品」の定義では、第1次機能(栄養)、第2次機能(味、香りなど)に加えて、第3次機能(生体防衛、疾病の予防、回復、体調リズムの調整、老化抑制など)の体調調節機能があるものとされており、「法律で定められた健康食品」よりは広い範疇の食品を含んでいるように思うのですが。
清水 「健康食品」も「いわゆる健康食品」も「機能性食品」も法律的には定義されていませんので、それぞれ使っている人によって少しずつニュアンスが違っています。「健康機能についての科学的な根拠があるもの」を、私は「機能性食品」と定義していて、大学や企業の研究者のほとんどの人がそういう意味で使っておられます。
「いわゆる健康食品」の中にも、科学的根拠があるものが含まれていますが、そうでないものもあり、さらに、そもそも「食品」のカテゴリーからもはみ出してしまっていて、法律的には「無承認無許可医薬品」ということで、薬事法違反になるものも含まれます。
岡部 図1の概念図でようやく何となく分かりました。それにしても、この分類方式は一般の人には、理解できないですね。どうしたらよいのですかね。
清水 専門家と言われる人たちがそれぞれ違った意味に使っているのを、「機能性食品」という用語の定義で統一するのは可能ですが、「健康食品」に加えて「いわゆる健康食品」なんていう言葉が一般化してきて、これがいっそう混乱を大きくしているのです。
岡部 法律で定められているのが「トクホ」と「栄養機能食品」しかなければ、そこからはみ出したもので、しかも健康によいと標榜しておれば「いわゆる健康食品」に入れるしかないわけですね。
他方、先生の図2にありますように、医薬品と機能性食品がダブる部分についても消費者には分かりにくいですね。
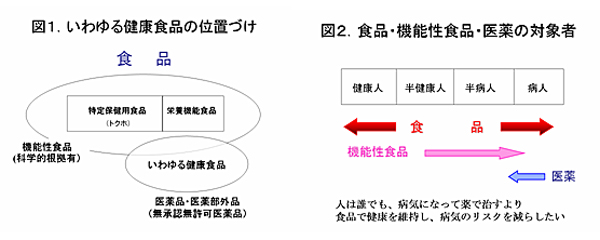
清水 業界サイドでは、機能性食品には病人にも有効であり、もっとはっきりした形の健康表示ができるようにしたいと要望はしているのですが、薬事法で医薬品に準ずるとされている医薬部外品など境界線上にある商品との関係については、問題が残っています。
岡部 それは、われわれ消費者にとっては迷惑な話ですね。たとえば、ビタミン類は、従来は医薬品か医薬部外品であったものが、今は、「栄養機能食品」として健康食品の方に入ってきています。それはよいとしも、医薬品とまったく同じ成分のものであっても、栄養機能食品には医薬品と同じ効能表示は許されていないというのは理解に苦しみます。
清水 栄養機能食品には、医薬品とか医薬部外品とまったく同じ効能表示はできません。ただ、われわれ食品側の人間としては、機能表示を認めてほしいということで厚労省に働きかけをして、ようやくトクホと栄養機能食品が実現したという思いが強いということです。もっとその範囲を拡大しようというのが、われわれの考えです。栄養機能食品にしても、ビタミンと5種類のミネラルだけではなく、ミネラルの種類を増やすとか、ハーブ類も入れるとかいった動きもあります。
〇特定保健用食品(トクホ)制度成立の経緯と現況
岡部 トクホは1991年に制定された「栄養改善法」によって制度化され、1997年には1,000億円程度であった市場規模が2007年には7,000億円にまで急成長し、認可品目数も2009年3月14日現在で845品目に達しています。
この間のご努力についてはよく分かりましたが、認可されたトクホの形態は、ヨーグルト、乳酸飲料、お茶などの通常の飲食物が大半を占めています。対象商品の種類が限定され、偏っているように感じるのですが、今後は拡大するのでしょうか。
清水 まず、健康によいかどうかを測定・評価する試験というのが実際にはなかなか難しいわけです。乳酸菌の種類にもいろいろあって、乳酸菌を一つのカテゴリーとして、一定の乳酸菌がこれだけ入っていれば、一定の効果があるということはなかなか言えません。乳酸菌の種類や食品の形態によっても違いますし、それを食べる人の食生活によっても違います。ですから、やはり個別の商品ごとに有効性の試験をして許可するしかないのです。
岡部 医薬品の場合には、副作用もあり、成分を厳密に特定することが不可欠ですが、ヨーグルトに含まれている乳酸菌やお茶に含まれているカテキンなどについて、そこまで厳密に個別の商品ごとに認定する必要があるのでしょうか。栄養機能食品では一定の成分含有が基準となっているわけですね。
清水 トクホにも定められた成分が一定量含まれているだけで表示のできる規格基準型のトクホが、最近新しく制度化されました。オリゴ糖と食物繊維はすでに許可を受けてから一定の期間が経って100くらいの商品が出たので、基準化された成分が入っているだけで「トクホ」として、定められた表示ができるようになっています。
岡部 ジェネリックと同じような考え方ですね。
清水 そうですね。オリゴ糖や食物繊維は、整腸の役割という意味で表示ができるようになったのですが、血糖値やコレステロール対応のトクホが100件を超えたので、次に規格基準型として認められるようになります。
岡部 トクホの場合には、そういう先発企業のイノベーション努力を評価する必要があるということですね。ただ、それが参入障壁にもなりますね。一つのトクホ開発にヒト試験まで行なって、科学的根拠をちゃんと揃えて、許可をとるのには、やはり最低でも1億円くらい掛かるでしょうから、中小企業ではできないことですね。
清水 そうですね。先発権が一定のプライオリティを保証されないと、研究が進みませんし、やはり一定の先発権を確保することは必要です。
岡部 その先発権に期限はあるのでしょうか。
清水 厳密な意味での先発権はありませんが、許可の期限について、トクホのスタート時には、4年の期限が定められていましたが、今は無期限になりました。その代わりに、同じ機能を持った個別商品の数が増えれば、「規格基準型」として認められるということになっています。規格基準型でも個別の商品ごとに許可をとる必要がありますが、費用は僅かで済みます。
岡部 規格基準型のトクホが増えてくれば、一定の成分が基準となるという点では、栄養機能食品と変わらなくなってしまうわけですね。
清水 それは、そうです。ただ、規格基準型になったのはまだ一種類の表示だけで、次に、血糖値低下機能のものが入ったとしても、二種類だけです。トクホの機能には10種類ありますから、全部が移行するのには相当時間が掛かります。一方、新しい機能の商品開発は、大会社中心になろうかと思いますが、いくらでも増やすことができますから、個別でトクホの許可を取得すれば、その機能分野ではかなりの期間、規格基準型にはならないということになります。
岡部 それは消費者にとってはあまり好ましいことではないですね。
清水 そういう面はありますが、新しい機能の許可を得るのにはかなりの開発費用が掛かるわけですから、企業にとってもすぐに追随されてしまうというのでは開発意欲が殺がれます。医薬品でも同じでしょうが、一定の先発権が保障されるような体制は必要ではないでしょうか。
岡部 トクホ商品の機能を特許権として保護することは考えられないのでしょうか。
清水 食品というのはもともと天然の既存物ですから、物質特許はとりにくいのです。物質特許の対象になるようなものは本当の新規成分ですから、安全性の面などで別の問題が出てきます。
岡部 それにして、トクホの品目数が実質的には10年余りの間に、845品目まで増えたのは、大変な勢いですね。
清水 総品目数は増えていますが、2003年に再許可という制度ができて、製品名を変更し、味とかフレーバーとか一部を変えたものは、事務局審査で簡単に許可される方式が可能となり、この再許可分が年間許可の半分を超えています。845品目のうちの3分の1くらいは新規性の乏しい後発品が占めており、まったく新しいものは減ってきています。
岡部 最近、食品の健康被害問題が増えていますが、トクホについて問題となったケースはないのでしょうか。
清水 安全性と有効性を評価したうえで、かなり限定的に個別に認められていますので、これまでのところトクホの健康被害というのは起きていないです。トクホはもともと食べていたものが中心ですから、量さえうまくコントロールできれば害にはならないのです。
岡部 こういう機能があると書かれているけれども、それは真っ赤な嘘だというようなクレームはないのでしょうか。
清水 それもあまりありません。実際に効いていない可能性はありますが。トクホをとった人からその効果があったかどうかを、①効いた、②効かない、③どちらでもない、④効果は気にしていないという四択でアンケートをとると、若い人が中心の場合には、70~80%の方から④の効果は気にしていないという回答が返ってきます。
これはどういうことかというと、医薬品は病気を治すのが目的で服用するわけで、効かないと困るが、食品はおいしいから食べる、飲料であれば喉が渇いているから飲むということで、直接的な効果はもともと期待していないと解釈できます。
岡部 ヨーグルトがおいしければ、健康増進に効いても効かなくてもよいということですね。
清水 味覚が主であって、それにプラスして、健康増進機能が補えればなおよいというのが消費者の考えではないでしょうか。
〇トクホの国際化と今後の課題
岡部 先生が努力を傾注されたトクホは、外国には広まらないのでしょうか。
清水 米国では1990年に、病気と食品との関係を表示できる制度ができ、94年にはサプリメント・タイプのものにも機能表示ができるようになりましたが、これは企業が実証したと考えれば自己責任で表示ができる制度で、わが国のトクホのように個別の商品ごとに行政の許可を得て、表示ができるという公的な裏づけはありません。一方、欧州では、わが国のトクホに近い制度をEUが制定することになり、2007年に法律が施行されて、現在、申請された表示の評価を行っており、2010年の1月に健康表示が公布される予定になっています。
岡部 EU案には、当初から特定商品許可型と規格基準型の双方が定められているそうですね。
清水 そうです。わが国と同じように行政機関である"European Food Safety Authority"(EFSA)が安全性と有効性の両方を評価して、健康表示ができるようになります。欧州はちょっと事情が複雑ですが、従来EU27カ国それぞれの国で別々に定められていた制度が統一されることに大きな意義があります。各国に業界自主基準はありましたが、1997年くらいから統一の話し合いは始まっていたので、各国は自国の健康表示に関して法制化を実施しないでいたのです。2007年に統一の法律ができて、やっとその評価が進められています。
この法律の考え方は、ヒトでのランダマイズ・コントロール・トライアル(RCT、無作為臨床試験)で有効成分を明確にして、製品が評価されてなければならないということで、基本的考え方はわが国のトクホと非常に似ています。
ですから、私は今、トクホをとっている日本企業にEUへも申請を出すように勧めています。そうすれば、日本企業がこれまで培ってきたトクホのサイエンスとレギュレーションを踏まえた申請資料が有効に使えます。
岡部 でも、特許権の保護がなければ、そういうノーハウを輸出するのは非常に難しいですね。食品会社が欧州でトクホのヨーグルトを現地生産するといったことは考えられるでしょうが。
清水 そうです。それは製品輸出でもよいし、現地生産も考えられます。製品ごとにヘルスクレーム(健康強調表示)を許可する制度ができるわけですから、最初はその製品にしか表示ができないのは、大きなメリットとなります。
岡部 トクホ製品が、国内だけではなく、大きな輸出商品に成長する可能性が出てきたのは、すばらしいことですね。
ところで、今後さらにトクホを健全な健康商品として育てる方策としては、どのようなことをお考えでしょうか。
清水 トクホは世界で最初に体の構造と機能に対して影響を及ぼすということが、食品に表示できるようになったもので、消費者にも受け入れられています。最近、頭打ちになっているのは、審査が、厳しくなり過ぎて、新規の機能表示がなかなか許可されないのが問題です。たとえば、3ヵ月のランダマイズ・コントロール・トライアル(RCT)で、プラセボとの間に、統計的有意差が2点ないといけないというのは、食品としての評価には重過ぎる負担です。
岡部 トクホは社会にも好意的に受け入れられ、安全性の問題も出ていないのになぜ、審査当局は規制を厳しく強化するのでしょうか。
清水 それは私の推測では、医薬品の方からの圧力が強まった結果です。トクホの売上が医薬部外品の売上を上回ってしまったので、これ以上、トクホが増えたら、これは大変なことだというのが医薬側の懸念で、厚労省に審査の厳格化を迫っているのです。もともと、厚労省の組織では、トクホの審査をする新開発食品保健対策室は生活衛生局にあったのですが、2001年にこれが医薬局に移されたのです。それからは、医薬側の考え方がトクホの審査に大きく影響を与えるようになってきたのです。
岡部 効能表示をする以上は。あまりいい加減な審査はできないというのは当然ですが、医薬部外品の売上がどんどん落ちてきたことが、トクホの成長を抑えているのは困ったことですね。
清水 そうなのです。医薬部外品との関係では、おかしな話がたくさんあります。たとえば、医薬部外品に対しては、眼精疲労とか、肩こりに対する効果などについて、ヒトでのランダマイズ・コントロール・トライアルによる検証がほとんど行なわれていないのです。一方、トクホには、ヒトでのランダマイズ・コントロール・トライアルが厳しく課されているのです。
岡部 それは、大きな矛盾ですね。そうすると、トクホの課題は食品との境界よりも、医薬部外品との境界に問題が移ってきた感がありますね。でも、たとえば、健康を維持するための予防目的での特定健康保健指導で、薬の服用を勧めるわけにはいかないですね。トクホを勧めるのは、理に適っているのでは。
清水 特定保健指導では薬は使わずに、食事指導と運動指導が中心ということになっていますが、基本的な考え方としてはあくまでも食事または食生活の指導であって、特定の健康食品を勧めることまでは含まれていません。
岡部 でも、トクホは行政が安全性と有効性を認めたものですから、指導する側とすれば、カロリー計算や単に白米ではなく玄米を食べなさいというだけではなく、機能の優れたトクホを勧めるところまで踏み込んでも問題はありませんね。
清水 そうです。そういう意味では、指導する人が一番安心して勧めることができるのはトクホということで、特定保健指導の中でトクホ商品を活かしていきたいというのは食品メーカーが考えていることです。それには一定の意味があると私は思っています。
〇「栄養機能食品」と「いわゆる健康食品」について
岡部 個別評価型のトクホと並ぶ機能性食品(健康食品)のジャンルとして、現在ビタミン12種類とミネラル5種類が規格標準型の「栄養機能食品」が認められ、それ以外は「いわゆる健康食品」と呼称されています。
栄養機能食品は、2001年の食薬区分の明確化により、従来医薬品扱いであったものが食品としてもその栄養素の機能表示が認められたものですが、同じ成分の物質が「医薬品扱い」であれば効能表示ができ、「食品扱い」の場合には認められないという制度には、消費者としては違和感を持ちます。この点はどうお考えでしょうか。
清水 規制する法律が異なるために、医薬品の表示と栄養機能食品の表示は違うということになっていますから、同じ成分のものが同じだけ入っていても、それが食品であるのか、医薬品であるのか、によって表示内容が異なります。これが、消費者が混乱する原因になっていると思います。
ただ、医薬品というのはもともと病気を治すためのもので、たとえばビタミンAが不足して夜盲症になっている方にビタミンAを大量に投与して、病気を治すために医薬品としてのビタミン剤があるわけです。その同じ成分が、健康維持のために栄養機能食品として使われているので、その部分が医薬品と食品のバッティング部分となるわけです。
岡部 なるほど。健康な人がビタミン剤を呑むのも自由ですが、健康維持の目的であれば別に詳しい効能表示の必要はないということですね。
清水 しかし、栄養機能食品でも、効能表示がないと一般の消費者にはビタミンB1にどういう機能があるのか分かりません。同じ成分のものが医薬品としても売られていると言う事実だけでは、消費者が栄養機能食品についてビタミンの機能を知ることはできず、不親切というこになります。
岡部 昔は過労で疲れてお医者さんに行くと、それではビタミン剤でも出しておきましょうかと処方してもらえたわけですが、今はビタミン剤なら自分で勝手に買って来なさいというだけのことですね。
清水 欠乏症という明確な病気が見つからなければ、まあ、そうですね。消費者にとっては、自分が不足している成分が自分の食生活の中から分かるようにすることが必要です。
岡部 自己責任と言われても、栄養機能食品以外のサプリメントには、健康増進には必ずしも役に立たない、中には害になる成分も含まれているようです。また、ビタミンのような栄養機能食品でも、摂り過ぎると無駄になる部分も非常に多いと思います。サプリメントの代金は100%自己負担ですから、消費者の勝手といえば勝手ですが。
清水 サプリメントという言葉は、"supplementation"で、そもそもは「補う」ということです。ですから、まず、第一に自分の食生活で何が不足しているのか、その不足しているものを、消費者が賢くなって分かるようになることが必要です。食品の代わりにサプリメントのかたまりをバッと食べるような人もいますが、それは賢い消費者とは言えません。
岡部 そこのところは難しいですね。サプリメント先進国である米国では、サプリメント一錠当たりの成分含有量が多く、値段は安いですね。一方、米国の消費者が格別に賢いとも思われませんが、米国ではサプリメントの過剰摂取や効能の虚偽表示などが問題にはなっていないのでしょうか。
清水 米国で販売されているサプリメントには必ず"This statement has not been evaluated by the FDA"という文言が印刷されています。要するに、ラベルに書いてある「機能表示」については、FDAは評価をしていませんということです。サプリメントの機能について法的には一切ギャランティーされていないのです。
それに、米国ではサプリメントの効能については、それぞれの企業が実証したと考えればよいわけで、その実証結果を公表することは義務づけられていません。ですから、機能については、昔から言われているとか、個人的な体験をベースにしたものが主であって、本当にヒトでの科学的エビデンスはないものが多く、大量に摂取することによる健康被害などの問題がたくさん出てきています。
岡部 わが国では、サプリメントの多くは「いわゆる健康食品」とされていますが、そのような問題はないのでしょうか。
清水 いや、もちろんあります。ただ、日本の場合はまだ量的には少ないということと、基本的には効能表示ができないということになっていますので、米国に比べると少ないのは事実です。それでも、動物試験しかしていなくて、副作用で重篤な被害が出たりしたケースもあります。
さきほどお話ししましたトクホについては、健康被害の報告は皆無ですが、「いわゆる健康食品」については健康被害が多発しています。もちろん、健康商品を摂取したことによって健康被害が発生したかどうかの因果関係の立証はなかなか難しいのですが。サプリメントでも、ハーブを入れたもので気管が閉塞して、重篤な病気になったようなケースも報告されています。
岡部 そうであれば、逆に言えば、ビタミンとかミネラルと同様にハーブ類も栄養機能食品として認めて、機能表示もある程度できるというふうにした方が消費者のためになりますね。
清水 それはそうです。できるものについては、少しずつ増やしていくというのが、規制緩和の趣旨にも合うわけです。しかしながら、米国ではハーブも含め、やたらに多くの種類のサプリメントが売られていますが、公的な裏付けはなく、健康被害も実際に多いのが問題であると考えられます。
岡部 サプリメントの市場規模は、どれくらいと見ておられるのでしょうか。
清水 なかなか推定が難しいですが、1兆円くらいはあるかも知れません。トクホ・栄養機能食品と合わせると、2兆円というところでしょうか。ただ、「栄養機能食品」と表示されているものの売上高は、せいぜい1,000億円程度です。公式統計はないので、おおよその数字ですが。
岡部 サプリメントの中でも、ビタミンとミネラルだけでは、そんなに小さい額ですか。それであれば、消費者の需要を満たし、安全を確保するためには、やはり栄養機能食品の成分の種類を増やすことが、なおさら必要ではないでしょうか。
清水 基本的には、私も栄養機能食品の種類を増やすことには賛成です。ただ、欧州でもハーブについては躊躇しています。なぜかというと、ハーブの中に入っている有効成分というのはなかなか一つ一つ同定できないのです。ハーブの成分は、その採れた場所とか、栽培の方法とか、最終的なエンリッチの方法によって、ものすごくぶれるのです。ですから、製品の評価が非常に難しいのです。また、有効成分が一つではなく、複数が絡み合っているので、どういう方法でヘルスクレーム(健康強調表示)と製品の有効成分との因果関係を科学的に証明するかが非常に難しいのです。
岡部 血圧を下げる効果があるとされている魚から抽出して造られるペプチドなどはトクホに入っていますが、「栄養機能食品」には入らず、ペプチドのサプリメントはできないわけですね。
清水 いや、そうでもありません。サプリメントの定義の問題ですが、サプリメントは「錠剤、カプセル状のもの」を指す場合と「いわゆる健康食品」と同じ意味で使われる2つの場合とがあります。前者の意味では、錠剤、カプセルの形状規制が2001年に撤廃されましたので、トクホでも商品ごとに評価されれば、錠剤、カプセルの形態も許可されるようになっています。
ですから、「栄養機能食品」となっているビタミン、ミネラル以外の成分のものについては、トクホの保健の用途と機能の表示の範囲をもっと拡大して、許可するべきだというのが私の考えです。それに、規格基準型のトクホも認められるようになったので、許可製品が多くなれば、栄養機能食品と同様に対応できます。
岡部 なるほど。トクホも活用して、標準的な均質の成分で割り切れるものは栄養機能食品で増やしていくという方向ですね。
〇健康食品承認制度の国際的動向とわが国のとるべき施策について
岡部 米国では、1994年制定の「栄養補助食品健康教育法(Dietary SupplementHealth and Education Act、 DSHEA)」により、「サプリメント」は食品、医薬品とは異なる第三のカテゴリーとして認められています。サプリメントの製造販売は「届出」が基本ですが、公的機関の監視体制は日本より厳しく、消費者にも情報公開されているので、安心感があるように感じていたのですが、実体はそうではないのですね。
清水 副作用がいろいろ問題になっており、安心感はありません。FDAは責任を負わないので、自己責任で判断しなさいといわれても、消費者にとってみると、機能についての科学的根拠の公開が企業に義務づけられていないので、調べようがないのです。
消費者が調べられない効果表示がされていて、情報を与えずに自己責任で選べというのでは、米国の消費者はかなり不利な状況に置かれています。そういう意味でも、米国の制度には大きな問題があるというふうに私は思っています。
岡部 米国の法律は、政府が責任を負わないことを明確にしているだけなのですね。私はこの法律で、ある程度、しっかり管理、規制されているのではないかと思っていたのですが。そうではないのですか。
清水 米国の法律は、"disclaimer"といって、政府が責任を持たないことの警告をはっきりさせているだけです。
岡部 FDAは管理しなくても業界団体とかで自主規制をしているのではないでしょうか。
清水 いや、有効性の科学的根拠については、それもありません。少なくとも、オーソライズされたものはありません。いろいろな業界団体があって、自主規制をする方向では検討されていますが、私から見ると、それは科学的根拠に基づくものとはとても言えないものです。
岡部 米国では、どの業界も儲け主義優先で、強欲が支配しているのですね。
清水 基本的には、そういうふうに考えてもよいと思います。
岡部 それにしては、米国の都市にはサプリメントだけの専門店が結構たくさんありますね。
米国はお手本にはならないとしても、サプリメントの形状は錠剤やカプセル状で、外見は医薬品と異ならないので、消費者重視の観点からは、わが国でもサプリメント独自の承認・監視法制を確立すべきではないでしょうか。
清水 規制の方向としては、私は欧州といかにハーモナイズするかを検討すべきではないかと考えています。今、EUで法制化されつつある食品の健康表示の制度がわが国とほぼ同じ考え方ですから、わが国もトクホの審査基準をもう少し食品の性格に合ったものに緩和するといた点をEUと議論するのが有益です。
岡部 なるほど。健康食品については、医薬品のように厳密でなくてもよいけれども、やはり科学的根拠をしっかり検証したうえで、ある程度の効果があって、安全性に問題がないというお墨付きを公的機関が与えないと、消費者は安心できませんね。
清水 そうです。EUは1997年から2004年にかけて2回のプロジェクトで機能性食品、ヘルスクレームについて検討を重ねてきました。その過程で、わが国にも何回か調べに来ました。私もEUの会議には参加をして、サイエンスとレギュレーションの関係など、わが国の考え方の紹介をしています。
岡部 欧州はわが国のシステムを勉強しているわけですね。
ところで、機能性食品に対する理解はかなり深まってきたようですが、一段と消費者に普及するには、どのような施策が必要とお考えでしょうか。
清水 最近では、医学系の先生方の中にも、数は少ないですが、病気の治療にも食品の機能を生かして行こうという考えの方が出てきましたので、この方向で今後も進められれば、機能性食品が普及すると思います。ただ、医学の問題は医学部では、栄養学が必須科目ではなく、「栄養学科」がないことです。唯一あるのは、徳島大学だけです。
たとえば、外科手術したとしても、その回復には栄養がすごく重要にもかかわらず、その栄養学を学んでいない医師が多いのです。
岡部 だから、医師は全部、栄養士に丸投げしてしまうわけですね。栄養士もカロリー計算が中心で、食品の多様な機能について医師にアドバイスできるレベルの方は少ないのでしょうね。
清水 そうです。栄養士が非常に低い位置に置かれていて、大学病院でも栄養士の部屋というのは地下の霊安室の隣とかにあって、その役割が軽視されています。
これを改善すべく、「管理栄養士」という栄養士より一つレベルの高い栄養士を育てるという制度がすでに作られています。さらに、管理栄養士よりももう一段高い大学院レベルの管理栄養士を育てようということが、日本栄養士会で今、検討されています。
岡部 栄養学会とか、栄養士の団体とかとは先生方の活動に非常にサポーティブなわけですか。
清水 そうですね。私は臨床栄養協会で役員もやっていますし、来年の臨床栄養学会との連合大会の臨床栄養協会大会の会長も務めることになっています。臨床栄養学会には、医師と栄養士の双方が入っていますが、この学会でも双方が対等の関係ができていない面もあります。
岡部 それはちょっと問題ですね。米国では、看護師、薬剤師、栄養士が医師と対等に議論するようになって来ていると聞いています。しかも、薬剤師の方が、医師よりもリスペクトされているという話ですが。
清水 まさに米国のよいところは、そこにあります。NST(Nutritionist Supporting Team)というのですが、医師と薬剤師と栄養士が一体になって患者のサポートをしていくというケア体制が、どこの病院でも出来上がっています。このNSTチーム内では、それぞれが独立の立場で意見をきちんと述べるのです。医師と薬剤師・栄養士は上下の関係ではなく、対等とのことです。こういう体制で医療が行われている米国は明らかにわが国より進んでいます。これはすばらしいことと思います。
岡部 やはり、わが国の問題はそこのところですね。よく分かりました。
本日は、目新しいお話をたくさんお伺いして、目から鱗でした。
(2009年7月13日、医療経済研究機構発行「医療経済研究機構レター(Monthly IHEP)」No.177、p1~13所収)
